- Microbiote

Groupe d’Etude des Tumeurs UroGénitales
Nous contacter
Actualités
Juillet 2024 : Journée Enseignement et Recherche du GETUG
Nous avons le plaisir de vous convier à la 8ème édition de la JER du GETUG qui se tiendra le 4 juillet au Rooftop 52 à Lyon.
Ne manquez pas cette nouvelle édition 2024 ! C’est une opportunité unique de rencontrer une communauté multidisciplinaire passionnée : oncologues médicaux et radiothérapeutes, urologues, médecins nucléaires, pathologistes, et bien d’autres.
Les inscriptions sont en ligne et disponibles ici !
Vous pouvez vous inscrire à distance ou en présentiel.
Attention, les inscriptions sont gratuites mais obligatoires.

RCP nationale CARARE (CAncers RAres du REin)
La eRCP nationale CARARE a pour objectif de discuter au niveau national, dans le cadre du soin, les cas de carcinomes du rein non à cellules claires métastatiques ou localisés et qui posent un problème de prise en charge (hors carcinomes rénaux à cellules claires). Elle est rattachée au réseau d’expert composé de 16 anatomopathologistes.
Elle se tiendra toutes les deux semaines, les mercredis à 17h30.
Téléchargez la procédure du RCP CARARE
Téléchargez le planning du RCP CARARE
Descriptif
Créé en 1994, le GETUG (Groupe d’étude des tumeurs urogénitales) est devenu le groupe coopérateur de référence dans son domaine.
Hébergé au sein d’Unicancer, il se consacre au développement de programmes de recherche en cancérologie et à la conduite d’essais cliniques dans les principaux cancers de l’appareil urologique et génitaux masculin.
Présidé par le Pr Karim Fizazi, oncologue médical à Gustave Roussy, le GETUG rassemble des experts issus de plusieurs spécialités : oncologues médicaux et radiothérapeutes, urologues, médecins nucléaires, anatomopathologistes et statisticiens.
Le GETUG dispose d’un vaste réseau d’hôpitaux universitaires, d’hôpitaux généraux, de CLCC et d’établissements privés, couvrant ainsi l’ensemble du territoire français.
Il est également amené à développer ou à participer à des projets de recherche à l’échelle internationale en étroite collaboration avec des groupes coopérateurs ou des universités en Europe, aux États-Unis ou en Australie (SOGUG, ICORG, EORTC, SAKK, MD Anderson, RTOG, UCL, ANZUP, etc.)
- 45 essais cliniques multicentriques nationaux et internationaux conduits par Unicancer depuis sa création
- 6 essais en cours d’inclusion, dont 3 essais internationaux
- 549 patients inclus en 2022 dans des essais promus par Unicancer
En 2010, un premier partenariat est établi avec l’AFU (Association Française d’Urologie) afin de mener conjointement des essais thérapeutiques nationaux et internationaux de phases II et III.
En 2018, l’intergroupe GETUG-AFU Alliance matérialise la collaboration entre les 3 groupes coopérateurs français impliqués dans la recherche clinique et translationnelle dans le domaine des cancers génito-urinaires : l’AFU (Association Française d’Urologie), le CeRePP (Centre de Recherche sur les Pathologies Prostatiques et Urologiques) et le GETUG. Ces groupes coopérateurs sont indépendants et appartiennent à des structures à but non lucratif, mais ont souhaité développer une entité commune pour potentialiser leurs programmes de recherches et leurs moyens opérationnels. Ainsi, après avoir engagé au cours des dernières années une démarche de structuration de la recherche en onco-urologie autour de deux objectifs principaux (essais cliniques et cohortes de patients associées à des bio-ressources), l’intergroupe GETUG-AFU Alliance souhaite poursuivre et amplifier les actions de recherche épidémiologique, biologique et interventionnelle dans le domaine des cancers génito-urinaires en s’appuyant sur les axes définis par l’INCa pour la stratégie décennale Cancer.
L’Institut national du cancer (INCa) a labélisé l’intergroupe GETUG-AFU-Alliance en 2018 et en a renouvelé ce label en 2022.
Le GETUG collabore aussi avec de nombreuses entreprises pharmaceutiques, comme AAA, AMGEN, ASTELLAS, ASTRA-ZENECA, BAYER, BMS, FERRING, IPSEN, JANSSEN, ROCHE, SANOFI, qui fournissent des traitements expérimentaux et des financements pour réaliser les essais cliniques.
Orientations stratégiques
La stratégie du GETUG se décline selon les axes suivants :
- Promouvoir des essais cliniques hautement compétitifs et susceptibles de modifier les pratiques mais aussi développer des programmes de recherche sur les tumeurs rares ;
- Valoriser les essais cliniques antérieurs ;
- Développer des programmes de recherche biologique au sein des essais cliniques ;
- Renforcer la visibilité du groupe à l’échelle nationale, via notamment l’intégration de jeunes chercheurs et le développement de task forces autour des enjeux actuels de la prise en charge des patients ;
- Renforcer les collaborations internationales avec le monde académique.
Gouvernance
Le GETUG agit sous la gouvernance d’un comité de pilotage composé de membres issus de diverses spécialités et ayant une expérience significative dans le domaine des essais cliniques portant sur les cancers uro-génitaux. Les membres de ce comité représentent les diverses institutions (CLCC, hôpitaux universitaires, hôpitaux privés) participant aux essais cliniques et à la définition de la stratégie du groupe.
Les principales missions du comité de pilotage sont de :
- Définir la stratégie du groupe
- Proposer et construire des essais cliniques et des enquêtes prospectives ou des études rétrospectives
- Valider la valeur scientifique des études
- Collaborer avec des groupes coopératifs internationaux
- Mener des études cliniques nationales et internationales en oncologie, répondre à des questions scientifiques sur les cancers urogénitaux
- Identifier et faire participer tous les experts du groupe à la conception des études

Pr Karim FIZAZI, Président du GETUG
Programme PEACE

Le programme PEACE : Consortium Européen sur le cancer de la prostate au profit de la Recherche
Le Consortium Européen sur le cancer de la prostate (PEACE : Prostate Cancer Consortium in Europe) a été créé en 2013. C’est un groupe de recherche paneuropéen ouvert à tous les spécialistes du cancer de la prostate exerçant dans les pays de l’Union Européenne. Les études nécessitant un nombre toujours plus important de patients, les spécialistes des cancers génito-urinaires se sont regrouper au sein d’organisations nationales et européennes contribuant ainsi de manière significative à la recherche et aux meilleures pratiques en matière de traitement des cancer génito-urinaires.
Depuis sa création, PEACE a ainsi permis la mise en place de plusieurs essais de phase III pour répondre à des questions sur l’utilisation de nouvelles options thérapeutiques pour les patients atteints du cancer de la prostate.
PEACE 1 (GETUG-AFU 21)
L’essai PEACE 1 est une étude prospective de phase III, randomisée, d’évaluation de l’association d’un traitement par déprivation androgénique avec docetaxel, avec ou sans radiothérapie, avec ou sans abiraterone et prednisone chez les patients présentant un cancer de la prostate métastatique hormono-naïf. Cette étude a été menée à l’échelle européenne (Allemagne, Belgique, Espagne, France, Irlande, Italie, Portugal, Roumanie, Suisse), dans lesquels 1 173 hommes ont été inclus entre novembre 2013 et décembre 2018.
Promotion : Unicancer
Sources de financement : Janssen Pharmaceutical NV, Ipsen, Sanofi, PHRC
(NCT01957436 ; EudraCT 2012-000142-35)
PEACE 2 (GETUG-AFU 23)
L’essai de phase III PEACE 2 porte sur le cabazitaxel et la radiothérapie dirigée vers les ganglions lymphatiques pelviens, chez des patients atteints d’un cancer de la prostate localisé et présentant au moins deux caractéristiques à haut risque de rechute. Cette étude a été menée à l’échelle européenne (Belgique, Espagne, France, Italie), dans lesquels 761 patients ont été inclus entre décembre 2013 et juillet 2021.
Promotion : Unicancer
Sources de financement : Astellas, Sanofi, PHRC
(NCT01952223 ; EudraCT 2012-000566-38)
PEACE 3
L’essai PEACE 3 est une étude multicentrique randomisée de phase III comparant l’enzalutamide et la combinaison de Ra-223 et d’enzalutamide chez les patients atteints de cancer de la prostate avec des métastases osseuses résistant à la castration asymptomatique ou modérément symptomatique.
Promotion : EORTC
(NCT02194842 ; EudraCT 2014-001787-36)
PEACE 4
L’essai PEACE 4 est une étude de phase III évaluant l’impact sur la survie de l’acide acétylsalicylique et l’atorvastatine chez les patients atteints de cancer de la prostate résistant à la castration. L’étude est en cours d’inclusion.
Promotion : Gustave Roussy
(NCT03819101 ; EudraCT 2017-004639-35)
PEACE 5
L’essai PEACE 5 est un essai de phase II coordonné en Belgique par l’Université de Ghent qui pose la question du traitement de rattrapage du cancer de la prostate en rechute ganglionnaire oligométastatique. L’étude est en cours d’inclusion.
Promotion : Université de Ghent
(NCT03569241)
PEACE 6 est un programme multi-essais :
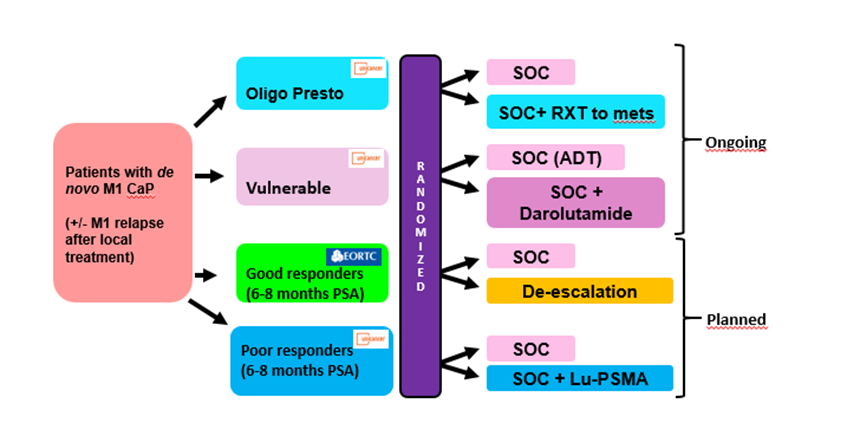
PEACE 6 OLIGO PRESTO (GETUG-AFU 36)
L’essai PEACE 6 OLIGO PRESTO est une étude randomisée de phase III évaluant le rôle du traitement ablatif local des métastases chez les patients atteints de cancer de prostate oligométastatique hormonosensible. Cet essai, en cours d’inclusion, est coordonné par le Prof Pierre Blanchard.
Promotion : Unicancer
Sources de financement : Janssen, PHRC
(NCT04115007; EudraCT 2017-A03104-49)
PEACE 6 VULNERABLE (GETUG-AFU 40)
L’essai PEACE 6 VULNERABLE est un essai de phase III randomisé en double aveugle évaluant l’efficacité de l’ADT ± darolutamide chez les patients atteints d’un cancer de la prostate de novo métastatique vulnérables avec une capacité fonctionnelle amoindrie et non éligibles au docétaxel ou aux agents ciblant les récepteurs aux androgènes. Cet essai clinique est en cours d’inclusion et sera mené dans une dizaine de pays au cours des prochaines années.
Promotion : Unicancer
Sources de financement : BAYER, PHRC
(NCT04916613 ; EudraCT 2020-003663-26)
PEACE 6 GOOD RESPONDERS (DE ESCALATE)
L’essai PEACE 6 GOOD RESPONDERS est un essai de phase III randomisé pragmatique évaluant une thérapie de privation androgénique intermittente à l’ère des inhibiteurs de la voie de signalisation des récepteurs des androgènes (AR). Le début des inclusions est prévu pour Q2 2024. L’étude prévoit d’inclure 1600 patients en Belgique, Espagne, France et Irlande.
Promotion : EORTC
(NCT05974774; EudraCT 2023-506817-23)
PEACE 6 POOR RESPONDERS (GETUG-AFU 42)
L’essai PEACE 6 POOR RESPONDERS est un essai randomisé de phase III évaluant l’efficacité du 177 Lu-PSMA-617 associé au traitement standard (SOC) par rapport au SOC seul chez des patients atteints d’un cancer de la prostate, de novo métastatique, hormonosensible avec un taux de PSA sérique ≥ 0,2 ng/ml. Le début des inclusions est prévu pour Q1 2024. L’étude prévoit d’inclure 500 patients en Belgique, Espagne, France, Irlande, Italie et Pays-Bas.
Promotion : Unicancer
Sources de financement : AAA/Novartis
(EudraCT 2022-502408-57-00)
PEACE 7 (GETUG-AFU 45)
L’essai PEACE 7 est un essai de phase III randomisée pour l’évaluation de l’efficacité du darolutamide et de la radiothérapie stéréotaxique chez des patients avec un cancer localisé de la prostate à haut risque de rechute. Le début des inclusions est prévu pour Q2 2024. L’étude prévoit d’inclure 700 patients en Espagne et France.
Promotion : Unicancer
Sources de financement : Bayer
(EudraCT 2023-509787-15-00)
PEACE 8 (GETUG-AFU 43)
L’essai PEACE 8 est un essai de phase III randomisée évaluant la combinaison darolutamide et radiothérapie stéréotaxique chez des patients atteints d’un cancer de la prostate résistant à la castration et présentant des oligométastases à l’imagerie fonctionnelle. Le début des inclusions est prévu pour Q2 2024. L’étude prévoit d’inclure 336 patients en Belgique, Espagne, France et Irlande.
Promotion : Unicancer
Sources de financement : Bayer
(EudraCT 2023-507482-26-00)
Projets phares hors programme PEACE
ALBAN (GETUG-AFU 37)
L’essai ALBAN est un essai de phase III, randomisé, en ouvert, évaluant l’efficacité de l’atezolizumab administré de manière concomitante à des instillations vésicales de BCG (Bacille de Calmette-Guérin) durant 1 an chez des patients atteints d’un cancer de la vessie non infiltrant le muscle, à haut risque de récidive et non préalablement traités par BCG. L’essai est mené en France, en Belgique et en Espagne. Le recrutement est terminé.
Promotion : Unicancer
Sources de financement : Roche
(EudraCT 2023-507482-26-00)
CARLHA 2
L’essai CARLHA 2 est un essai de phase III, randomisé, en ouvert, évaluant l’efficacité de l’association apalutamide avec une radiothérapie et un agoniste de la LHRH chez des patients atteints d’un cancer de la prostate à haut risque de récidive biochimique après prostatectomie. L’étude est en cours d’inclusion.
Promotion : Unicancer
Sources de financement : Janssen Pharmaceutical NV
(EudraCT 2017-000155-21)
Synopsis des études en cours d’inclusion
Comment proposer un projet de recherche ?
Les critères d’acceptation/refus d’une étude/d’un essai à développer au sein du GETUG sont transparents :
- Adéquation ou non à la stratégie du groupe
- Innovation et originalité
- Faisabilité médicale, technique et financière
La proposition doit être rédigée sous la forme d’un synopsis, adressé par e-mail au responsable du programme clinique d’Unicancer
Le synopsis doit comprendre : titre et acronyme, objectifs, critères d’évaluation, critères d’inclusion et d’exclusion, plan de l’étude, traitements à l’étude s’il y a lieu, contexte scientifique, hypothèses statistiques, coûts estimés (si disponibles) et type de soutien financier envisagé.
Le synopsis doit être rédigé en anglais.
Le responsable du projet sera invité à présenter sa proposition lors d’une réunion du comité de pilotage ou d’une Assemblée Générale. Après validation, l’essai peut être mis en place avec l’aide de l’équipe projet d’Unicancer.
Si vous souhaitez proposer un projet de recherche au GETUG, merci de contacter Mme Catherine Léger, Responsable du Groupe d’experts, à
Communications et publications

4 publications en 2023

4 communications orales lors de congrès en 2023
La communication des résultats des études prospectives conduites par le GETUG, lors de congrès internationaux majeurs ainsi que dans des revues à « fort facteur d’impact », a permis au groupe d’acquérir une large visibilité internationale au fil des ans et de mener des essais à l’échelle européenne (programme PEACE – Prostate cancer Consortium in Europe), comme les essais PEACE 1 et PEACE 2, dirigés par le Professeur Karim Fizazi.
Retour sur les Journées d’Enseignement Recherche du GETUG (replay)
JER 2023
Retrouvez le replay complet de la Journée Enseignement & Recherche 2023 du GETUG
Replay par sessions
- Session 1 – Controverses actuelles en cancérologie génito-urinaire
- Session 2 – PSMA et médecine nucléaire en cancérologie génito-urinaire
- Session 3 – Prise en charge du patient âgé en cancérologie génito-urinaire
- Session 4 – Travaux sur le CTDNA
- Session 5 – Prise en charge du cancer du rein comment faire mieux avec l’arsenal thérapeutique actuel

